«MitoCatch» liefert gesunde Mitochondrien an erkrankte Zellen
Bei zahlreichen Erkrankungen spielen geschädigte Mitochondrien eine zentrale Rolle. Diese kleinen Strukturen dienen der Energieversorgung von Zellen. Forschende stellen nun das System «MitoCatch» vor, das gesunde Spender-Mitochondrien gezielt in die Zellen bringt, die sie am dringendsten benötigen.
15. April 2026
Funktionsstörungen der Mitochondrien liegen vielen bislang unheilbaren Krankheiten zugrunde. Dazu gehören neurodegenerative Krankheiten wie Parkinson, Degeneration des Sehnervs und bestimmte Formen von Herzinsuffizienz. Bisherige Versuche, gesunde Mitochondrien in geschädigte Zellen zu transplantieren, sind oft ineffizient. Sie können zudem nicht garantieren, dass die neuen Mitochondrien auch wirklich dort ankommen, wo sie am dringendsten gebraucht werden.
Forschende unter der Leitung von Prof. Dr. Botond Roska am Institut für Molekulare und Klinische Ophthalmologie Basel (IOB) und der Universität Basel berichten nun im Fachjournal «Nature» von einer neuen Technologie namens «MitoCatch». Mit dieser lassen sich Mitochondrien von gesunden Spenderinnen und Spendern gezielt in die Zellen einbringen, die am stärksten von Krankheiten betroffen sind. Mit diesem innovativen Ansatz rückt die Behandlung von Erkrankungen, bei denen geschädigte Mitochondrien eine zentrale Rolle spielen, in greifbare Nähe.
Verkuppler für Mitochondrien und Zellen
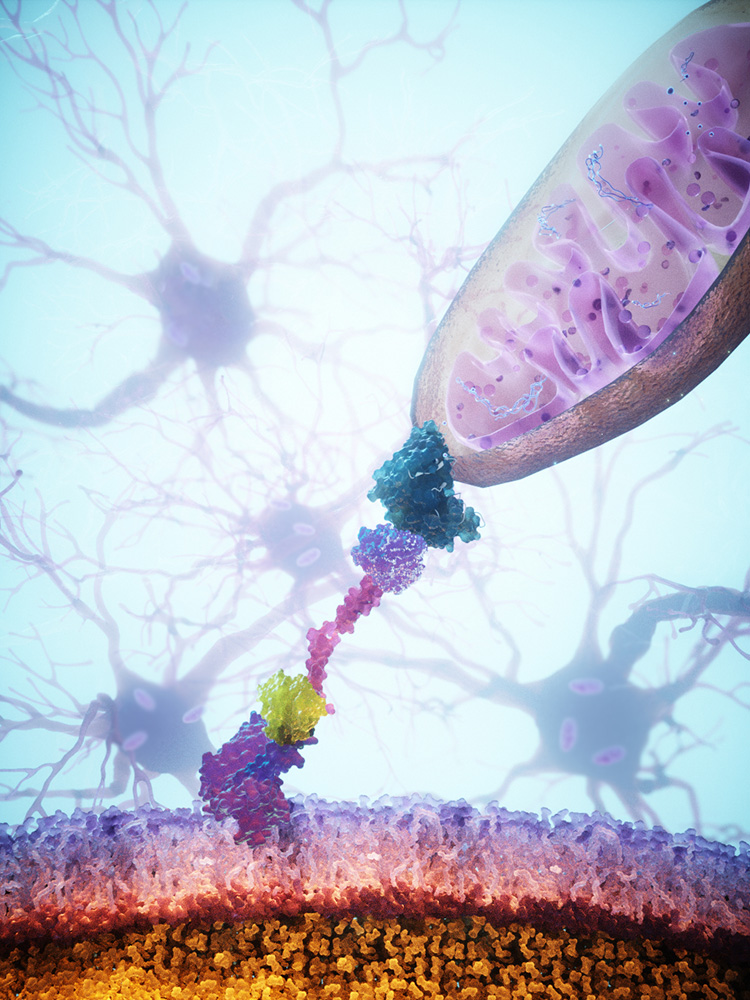
Das System «MitoCatch» basiert auf gentechnisch entwickelten Andockhelfern (Proteinen), die Mitochondrien gezielt in die richtigen Zellen lotsen. Die Forschenden des IOB und der Universität Basel haben dafür drei unterschiedliche Strategien entwickelt: Bei «MitoCatch-C» werden die Zielzellen mit Andockhelfern auf der Zelloberfläche ausgestattet, so dass die neuen Mitochondrien sich daran anheften und in die Zelle aufgenommen werden können. Das setzt allerdings voraus, dass man die Zielzellen ausserhalb des Körpers entsprechend verändern und wieder in den Organismus zurückschleusen kann.
Beim Ansatz «MitoCatch-M» ist das nicht nötig: Angepasst werden hierbei die Spender-Mitochondrien. Sie erhalten Andockhelfer, die sie zu den richtigen Zielzellen lotsen und nur dort anheften lassen. Bei der dritten Variante «MitoCatch-Bi» bleiben sowohl Zielzellen als auch Spender-Mitochondrien unverändert, vielmehr dient ein bispezifischer Andockhelfer als Brücke, die die Mitochondrien mit der Zelloberfläche verbindet. Durch die gezielte Anpassung dieser Andockhelfer lässt sich steuern, wie effizient und selektiv die Mitochondrien verschiedene Zelltypen erreichen.
Das Team um Temurkhan Ayupov und Dr. Verónica Moreno-Juan, Co-Erstautor und -Erstautorin, testete das System an verschiedenen Zelltypen, sowohl von Mäusen als auch von Menschen. Es zeigte sich, dass «MitoCatch» Mitochondrien zuverlässig in Neuronen sowie in Netzhaut-, Herz-, Endothel- und Immunzellen bringt. Einmal in der Zelle angekommen, bleiben die Mitochondrien funktionsfähig. Sie bewegen sich, fusionieren und teilen sich, was für das normale Energiemanagement einer Zelle entscheidend ist.
Ansatz für geschädigte Sehnerven und Netzhaut
Das Forschungsteam konnte ausserdem an Gewebeproben von Verstorbenen zeigen, dass Spender-Mitochondrien das Überleben von Neuronen verbessern, die von Personen mit Erkrankungen des Sehnervs stammen, und gleichzeitig die Regeneration von Ganglienzellen der Netzhaut nach Verletzungen fördern. In Tiermodellen wird die Methode bisher gut vertragen, ohne nachweisbare Abwehrreaktion des Immunsystems.
«MitoCatch» schafft einen völlig neuen Ansatz für präzise mitochondriale Medizin. Die Technologie überwindet eine langjährige Hürde, Spender-Mitochondrien spezifisch in erkrankte Zellen einzubringen, und könnte so die Behandlung mitochondrialer Erkrankungen revolutionieren.
Dieser Artikel beruht auf einer Medienmitteilung des IOB.
Originalpublikation
Temurkhan Ayupov, Verónica Moreno-Juan et al.
Cell-type-targeted mitochondrial transplantation rescues cell degeneration
Nature (2026), doi: 10.1038/s41586-026-10391-0