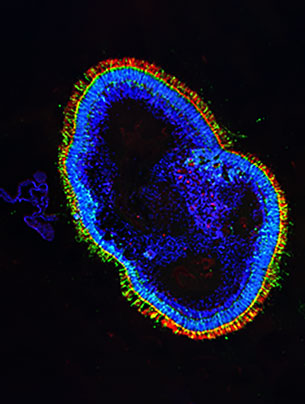
Neue Netzhaut aus einer Hautprobe.
Text: Christoph Dieffenbacher
Um bestimmte Augenkrankheiten zu verstehen, bauen Forschende die menschliche Netzhaut im Labor nach. Dafür stellen sie sogenannte Organoide mit körpereigenen Zellen aus Haut und Blut her.
Das Spezialgebiet der jungen Österreicherin Magdalena Renner sind sogenannte Organoide. Das sind Kleinstorgane aus wenigen Zellen, die in einer Kultur mittels umprogrammierter Stammzellen künstlich erzeugt werden und heranwachsen. Für ihr Doktorat in Wien hatte die Molekularbiologin mit Gehirnorganoiden gearbeitet, aus wenigen Zellen kleinste Gehirne nachgebaut und ihre Entwicklung beobachtet.
Heute leitet sie am Institut für Molekulare und Klinische Ophthalmologie in Basel (IOB) eine Gruppe, die sich mit Organoiden der Netzhaut beschäftigt. Ziel ihrer Arbeiten zwischen Grundlagenforschung und angewandter Forschung ist es, verschiedene Augenkrankheiten besser zu verstehen. Ihrem Team ist es bereits gelungen, relativ hoch organisierte Formen der menschlichen Netzhaut im Labor heranwachsen zu lassen.
Kompliziertes Nervengewebe
Nun ist die Netzhaut, eine Art mehrlagige Tapete an der Innenseite des Auges, alles andere als ein einfaches Organ, sondern ein äusserst komplexes Gewebe: «Hier finden sich zahlreiche Zelltypen mit unterschiedlichen Funktionen, die erst noch in fünf verschiedenen Schichten angeordnet sind», erklärt Renner. Genauer gesagt sind es drei Schichten mit Zellkörpern und zwei Zwischenschichten, in denen sich zwischen den Nervenzellen Synapsen befinden. In Organoiden wie in der menschlichen Retina sind die Fotorezeptoren in der obersten Zellkörperschicht. Die Fotorezeptoren beim Menschen nehmen jeweils die einfallenden Lichtsignale auf und leiten sie als Impulse ans Gehirn weiter.
Eine solche komplexe Struktur macht die Netzhaut, lateinisch Retina («Netz»), denn auch besonders sensibel – die meisten Augenkrankheiten nehmen hier ihren Anfang. Zu den häufigsten Krankheiten, von denen ein Teil vererbbar ist, gehören etwa die altersbedingte Makuladegeneration, die diabetische Retinopathie, Gefässverschlüsse und die Netzhautablösung. Die grosse Anfälligkeit der Netzhaut illustriert Renner an einem Beispiel: «Bereits wenn ein einziges Gen in den Fotorezeptoren nicht funktionsfähig ist, kann jemand erblinden.» Falls sich nun die Entwicklung der Netzhaut und die möglichen Genmutationen bei bestimmten Krankheiten im Labor modellieren liessen, wäre das ein wichtiger Schritt in Richtung neue Therapien – davon sind viele Forschende überzeugt.
«Unsere Organoide der Netzhaut gleichen dreidimensionalen Miniorganen, die fast so aussehen und ähnlich aufgebaut sind wie die Originale», erläutert die Forscherin in ihrem Labor. Nur etwa zwei mal zwei Millimeter messen die Kleinstorgane, dann hören sie auf zu wachsen. Die Organoide enthalten ähnliche Zelltypen mit denselben oder verwandten Funktionen wie die ausgewachsene Netzhaut. Renner erklärt: «Wir beginnen in der Regel mit einer Spenderzelle aus einer kleinen Biopsie der Haut oder, weniger invasiv, aus einer Blutprobe. Diese werden in sogenannte induzierte pluripotente Stammzellen umprogrammiert, eine Methode, die es erst seit etwa zwölf Jahren gibt.» Die Stammzellen, die sich in alle möglichen Körperzellen differenzieren lassen, werden daraufhin angeregt, sich zu vermehren.
Auge als Teil des Gehirns
Die ersten Ergebnisse ihrer Forschungen hätten sie selbst überrascht, erzählt die Wissenschaftlerin rückblickend: «Der Prozess, den die Stammzellen in der Laborkultur durchmachen, entspricht ziemlich genau der natürlichen Entwicklung der Netzhautzellen im menschlichen Embryo.» So entwickeln sich die Retinazellen zunächst wie Gehirnzellen allgemein, bevor sie sich später spezialisieren. «Ist ja klar», sagt Renner, «das Auge ist nun einmal ein Teil des Gehirns.» Während der Entwicklungsspanne der Organoide haben die Forschenden zu unterschiedlichen Zeitpunkten Organoide in einzelne Zellen zerlegt, diese aufgelöst und die RNA von 60 000 einzelnen Zellen untersucht. Damit konnten sie Rückschlüsse darauf ziehen, welche Gene in den unterschiedlichen Zelltypen exprimiert wurden. Ziel ist es, möglichst zu reifen Netzhautzellen zu kommen.
Neben den Zellkulturen erforscht Renners Gruppe auch die Netzhaut von Organspendern, analysiert sie punkto Genexpression und vergleicht sie mit jenen der im Labor gezüchteten Organoide. Dabei zeigte sich, dass ein Grossteil der bekannten Gene, die mit erblicher Netzhautdegeneration im Zusammenhang stehen, von bestimmten Zelltypen exprimiert werden. «Diese Erkenntnis ist wichtig, da wir zuallererst die von einer Mutation unmittelbar betroffenen Zellen behandeln wollen», sagt die Forscherin.
Wie schwierig ist es, die menschliche Retina in Kultur nachzubauen? Das Hauptproblem sei, sagt Renner, dass die Reifung der Netzhaut mehr als 30 Wochen dauert, was für die Forschung einen sehr grossen Zeitraum und einen immensen Aufwand bedeutet. Daher müsste die Gruppe ihre Experimente auch sehr lange im Voraus planen – und viel Geduld haben. Ein noch nicht gelöstes Problem sei etwa, dass nicht alle Zellen desselben Typs auch gute Organoide bilden.
Mausmodell im Nachteil
Doch dass mit künstlich hergestelltem Gewebe Teile der Retina gezielt repariert oder gar Krankheiten beim Menschen geheilt werden können – bis dahin ist es wohl noch ein weiter Weg. Anders als die Hornhaut lässt sich die Netzhaut nämlich nicht einfach transplantieren. Erprobt wird daher, Zellen, die durch eine erblich bedingte Mutation eine fehlerhafte Funktion aufweisen, mit einer korrekten Kopie des Gens zu versorgen und somit wieder funktionsfähig zu machen. Dafür werden die infrage kommenden Retina-Genabschnitte in Viren verpackt und diese in den Augenhintergrund gespritzt – ein Therapieansatz, der sehr einfach in Organoiden getestet werden kann. Die Methode sei erfolgversprechend, so Renner, weil das Auge vom Immunsystem wenig überwacht, ein eindringender Virus also nicht sofort bekämpft werde.
Die mögliche Anwendung und der Einsatz von neuen Therapien, die mit Organoiden entwickelt werden, müssten später auch am Tier getestet werden, sagt Renner. Dabei habe das in den Labors häufig angewendete Mausmodell in der Augenforschung einen grossen Nachteil: «Mäuse sehen ganz schlecht, denn ihre Retina weist eine andere Struktur auf als jene des Menschen.» Bei uns befindet sich im Zentrum der Netzhaut die sogenannte Fovea, eine Region mit speziellen Fotorezeptoren, die für das Farbenerkennen und das scharfe Sehen wichtig sind. Bei Mäusen fehlt sie. Nur bei einigen Primaten gebe es die Fovea noch, sodass sich entsprechende Versuche wohl nicht ganz vermeiden lassen, sagt die Forscherin. Möglich sei aber, dass ein grosser Teil der Tierversuche dereinst durch Organoide ersetzt werden könnten.
Weitere Artikel in der aktuellen Ausgabe von UNI NOVA.