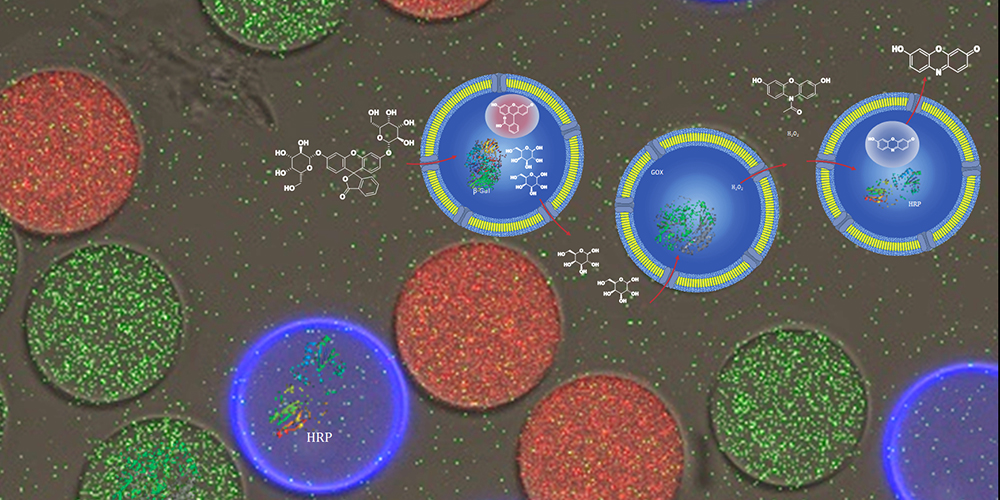
Die künstliche Zelle auf einem Chip
Forschende der Universität Basel haben ein exakt kontrollierbares System entwickelt, um biochemische Reaktionskaskaden in Zellen nachzuahmen. Sie nutzen die Mikrofluid-Technik um Mini-Reaktionscontainer aus Polymeren herzustellen, die sie mit den gewünschten Eigenschaften ausstatten. Nützlich ist diese «Zelle auf einem Chip» nicht nur für die Erforschung von Prozessen in Zellen, sondern auch für die Entwicklung neuer Synthesewege für chemische Anwendungen oder für biologische Wirkstoffe in der Medizin.
28. Oktober 2020
Um zu überleben, zu wachsen und sich zu teilen, sind Zellen auf eine Vielzahl verschiedener Enzyme angewiesen, die zahlreiche aufeinander folgende Reaktionen katalysieren. Wann bestimmte Enzyme in welchen Konzentrationen vorliegen und welches das optimale Mengenverhältnis zwischen ihnen ist, lässt sich aufgrund der Komplexität der Vorgänge in lebenden Zellen nicht bestimmen. Stattdessen dienen einfachere, synthetische Systeme als Modelle für die Untersuchung dieser Prozesse. Die synthetischen Systeme simulieren dabei die Unterteilung lebender Zellen in Kompartimente, also voneinander abgegrenzte Bereiche.
Grosse Ähnlichkeit mit natürlichen Zellen
Das Team von Prof. Dr. Cornelia Palivan und Prof. Dr. Wolfgang Meier vom Departement Chemie der Universität Basel hat nun eine neue Strategie zur Herstellung derartiger synthetischer Systeme entwickelt. Sie produzieren dazu verschiedene synthetische Mini-Reaktionscontainer, Vesikel genannt, die in ihrer Gesamtheit als Zellmodelle dienen. Davon berichten sie im Fachjournal «Advanced Materials».
«Wir stützen uns hierbei nicht wie früher auf die Selbstorganisation der Vesikel, sondern haben eine effiziente Mikrofluid-Technik entwickelt, um enzymbeladene Vesikel kontrolliert zu produzieren», erläutert Wolfgang Meier. Die Grösse und die Zusammensetzung der Vesikel lassen sich mit der neuen Methode gezielt steuern, sodass in den unterschiedlichen Vesikeln dann - ähnlich wie in unterschiedlichen Kompartimenten einer Zelle – verschiedene biochemische Reaktionen ablaufen können ohne sich gegenseitig zu beeinflussen.
Für die Herstellung füllen die Forscher die verschiedenen Komponenten der gewünschten Vesikel in winzige Kanäle auf einem Silizium-Glas-Chip. Auf dem Chip treffen sich alle Mikrokanäle an einer Kreuzung. Unter den richtigen, einstellbaren Bedingungen bilden sich am Kreuzungspunkt der Kanäle gleichgrosse Polymertropfen, die in einer wässrigen Emulsion schwimmen.
Präzise kontrollierbar
Die Vesikel bestehen aus einer Polymermembran als Hülle und einer wässrigen Lösung im Inneren. Gleich bei der Herstellung werden die Vesikel gezielt mit unterschiedlichen Enzymkombinationen gefüllt. «Mit dieser neu entwickelten Methode können wir massgeschneiderte Vesikel herstellen und die gewünschte Konzentration der enthaltenen Enzyme genau einstellen", fasst Dr. Elena C. dos Santos, Erstautorin der Studie, die entscheidenden Vorteile zusammen.
In die Membran integrierte Proteine fungieren als Poren und ermöglichen den spezifischen Ein- und Austritt von Verbindungen in und aus den Polymervesikeln. Die Porengrössen sind dabei so bemessen, dass sie nur die Passage spezifischer Moleküle oder Ionen erlauben. Prozesse, die in der Natur eng nebeneinander in einer Zelle ablaufen, lassen sich so getrennt untersuchen.
«Wir konnten zeigen, dass das neue System eine gute Grundlage bietet, um enzymatische Reaktionsprozesse zu untersuchen», erklärt Cornelia Palivan. «Sie lassen sich optimieren, um die Produktion eines gewünschten Endprodukts zu erhöhen. Zudem sind wir mit der Technik in der Lage spezifische Mechanismen genau zu untersuchen, die bei Stoffwechselkrankheiten eine Rolle spielen oder die Umsetzung bestimmter Medikamente im Körper betreffen.»
Die Arbeiten wurden vom Swiss Nanoscience Institute der Universität Basel, dem Schweizerischen Nationalfonds und dem Nationalen Forschungsschwerpunkt «Molecular Systems Engineering» unterstützt.
Originalpublikation
E. C. dos Santos, A. Belluati, D. Necula, D. Scherrer, C. E. Meyer, R. P. Wehr, C. G. Palivan, W. Meier
Combinatorial strategy for studying biochemical pathways in double emulsion templated cell-sized compartment
Advanced Materials (2020), DOI: 10.1002/adma.202004804
Weitere Auskünfte
Prof. Dr. Cornelia G. Palivan, Universität Basel, Departement Chemie, Tel. +41 61 207 38 39, E-Mail: cornelia.palivan@unibas.ch
Prof. Dr. Wolfgang P. Meier, Universität Basel, Departement Chemie, Tel. +41 61 207 38 02, E-Mail: wolfgang.meier@unibas.ch